Освоить
фотографию в наш век — дело более чем нехитрое. Оно, пожалуй, под силу и
октябренку. Пусть он не будет знать всех тайн фотографического
процесса. (Между нами говоря, кое-что неясно даже специалистам.) Но
снимать и проявлять — тут требуется лишь небольшая практика да несколько
добрых советов взрослых.
А поэтому мы не будем расписывать в подробностях, что нужно делать фотографу.
Он, например, хорошо знает, что иногда
фотографии покрываются бурыми пятнами. Особенно когда они лежат на свету
и долго хранятся. «Стало быть, — скажет фотограф, — в процессе
проявления бумаги (или пластинки) изображение недозакрепилось».
По-научному это значит: пластинку или фотобумагу недостаточно держали в фиксирующем растворе.
Зачем нужен фиксаж? И на этот вопрос легко ответит всякий, кто хоть немного увлекался фото.
Чтобы удалить с поверхности пленки остатки бромистого серебра, которое не разложилось при действии света.
Фиксажей изобретено немало. Но самый дешевый, самый популярный из них — гипосульфит. Химики называют его тиосульфатом натрия.
Но сначала о сульфате. Он известен
давным давно, и открыл его немецкий химик Иоганн Глаубер. Поэтому
сульфат натрия именуют еще и глауберовой солью. Его формула Na2SO4 · 10H2O.
Химики любят изображать соединения в виде структурных формул. Безводный сульфат натрия они нарисуют так: И
даже новичок в химии, взглянув на формулу, легко увидит: сера здесь
положительно шестивалентна, кислород — отрицательно двухвалентен.
Тиосульфат построен почти так же. За исключением одной детали — вместо атома кислорода стоит атом серы:
 или так: или так: 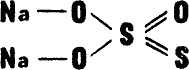
Просто? Конечно. Но до чего же все-таки
любопытное соединение этот тиосульфат! Оно содержит два атома серы
разной валентности. Один несет заряд 6+, другой 2–. Не так уж часто
сталкиваются химики с подобным явлением.
Даже в самом обыденном нередко кроется необычное.
|  З В О Н О К НА У Р О К
З В О Н О К НА У Р О К З В О Н О К НА У Р О К
З В О Н О К НА У Р О К