|
Наша планета окружена атмосферой — воздушной оболочкой,
простирающейся от поверхности Земли более чем на полторы тысячи километров.
Масса этого воздушного океана внушает уважение — 5•1015 т! Воздух
представляет собой сложный, многокомпонентный газовый «коктейль», который
помимо основных составляющих — азота и кислорода — включает аргон, углекислый
газ, водяные пары, мельчайшие твёрдые частицы (пыль), капельки воды, а также
незначительные примеси многих других веществ (SO2, CH4, NH3, СО, HF, H2, H2S и т. д.).
Важнейшей частью воздуха является кислород, необходимый
для дыхания как животным, так и растениям.
Вдыхаемый нами кислород идёт на окисление сложных
органических молекул — углеводов и жиров — до углекислого газа и воды. Эти
реакции сопровождаются выделением и накоплением энергии и протекают с участием
белковых катализаторов -ферментов (см. статью «Ферменты -на все руки мастера»).

Состав атмосферы Земли.
К моменту появления человека углекислый газ, так
необходимый растениям, уже стал дефицитом. Его концентрация в воздухе до
начала промышленной революции составляла всего 0,029%. Однако в последние полтора
столетия из-за сжигания ископаемого топлива и уничтожения лесов содержание СО2
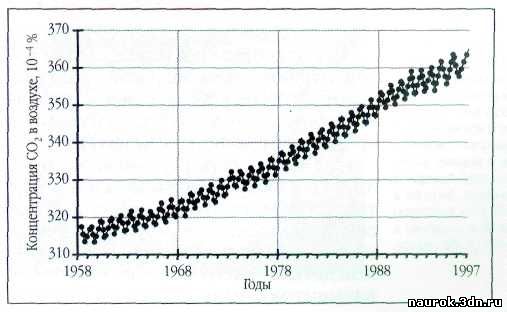
в атмосфере повышается. По данным американской обсерватории Мауна-Jloa (Гавайские острова), только с 1958 по
1997 г. среднегодовая концентрация СО2 в воздухе выросла с 0,0315 до
0,03б5%.
Находящиеся в воздухе азот и аргон играют роль
балласта, а содержание других газов совсем незначительно и измеряется сотыми
и тысячными долями процента.
Два самых лёгких — водород и гелий — не могут
удерживаться земным тяготением, поэтому, попав в атмосферу (водород — в
результате вулканической деятельности, гелий — вследствие распада
радиоактивных элементов), они довольно быстро улетают в космос. Аммиак NH3 и хлороводород очень хорошо растворяются
в воде, поэтому с дождями они попадают в почву, где аммиак усваивается
растениями, а хлороводород реагирует с минеральными веществами. Сероводород
под действием света окисляется до оксида серы(IV): 2H2S+3О2= 2Н2О+2SO2, который в присутствии кислорода
воздуха и паров воды превращается в серную кислоту. Последняя в значительной
степени нейтрализуется присутствующим в воздухе аммиаком.
|  З В О Н О К НА У Р О К
З В О Н О К НА У Р О К З В О Н О К НА У Р О К
З В О Н О К НА У Р О К