|
Если капельку воды нанести на стекло и подождать, пока
она испарится, то на месте капли будут видны белые разводы — это
кристаллизуются растворимые в воде соли. Содержание солей в природных водах
различается в тысячи раз. Например, в литре дождевой воды содержатся единицы,
максимум десятки миллиграммов солей. А в литре воды из залива Кара-Богаз-Гол
(Каспийское море) — 300 г, почти треть от массы раствора.
В водных растворах подавляющее большинство солей
существует в виде ионов.
В природных водах преобладают три аниона (гидрокарбонат
НСО-3, хлорид Cl- и сульфат SO2-4) и
четыре катиона (кальций Са2+, магний Mg2+, натрий Na+ и калий К+) — их называют главными ионами. Хлорид-ионы придают
воде солёный вкус, сульфат-ионы, ионы кальция и магния — горький,
гидрокарбонат-ионы безвкусны.
Гидрокарбонат-ионы нейтрализуют кислоты, попадающие в
водоём с атмосферными осадками или образующиеся в результате жизнедеятельности
организмов: Н++НСО-3=Н2О+СО2. С
концентрацией гидрокарбонат-ионов напрямую связана устойчивость водоёмов к
кислотным дождям. Наиболее чувствительны к ним реки и озёра Карелии, Финляндии,
Скандинавии, в водах которых этих ионов практически нет.
Ионы попадают в водоёмы из трёх источников. Первый
источник — атмосферные осадки, формирующиеся над океанами. Штормовой ветер срывает
с водной поверхности мельчайшие капельки, а затем воздушные потоки переносят
их на тысячи километров. Поскольку морская вода содержит в основном ионы Cl-
и Na+, их с
осадками выпадет больше всего — несколько тонн на 1 км2 за год. В
реки и озёра Европейской России 2/3 всех хлорид-ионов поступают с дождём и
снегом.
Второй источник солей — горные породы. Часть воды,
выпавшей в виде осадков, впитывается в грунт, а из него попадает в реки. При
этом многие компоненты грунта реагируют с водой или с растворённым в ней углекислым
газом. Так, известняк легко образует растворимый (до 1,6 г/л) гидрокарбонат
кальция: СаСО3+Н2О+СО2=Са(НСО3)2.
Почти на всей европейской части России (кроме Карелии и Мурманской области)
известняки, а также доломиты MgCO3•СаСО3
залегают довольно близко к поверхности. Поэтому вода здесь содержит преимущественно
гидрокарбонаты кальция и магния. В таких реках, как Волга, Дон, Северная Двина,
и основных их притоках гидрокарбонаты кальция и магния составляют от 3/4 до
9/10 всех растворённых солей.
Соли попадают в водоёмы и в результате деятельности
человека. Так, хлориды натрия и кальция зимой в изобилии сыплют на дороги,
чтобы растапливать лёд. За один сезон на 1 м2 дорог приходится до
100 кг соли. Весной вместе с талой водой она стекает в реки. Треть хлоридов в
реках европейской части России привнесена туда человеком. В реках, на которых
стоят крупные города, эта доля гораздо больше. Например, концентрация хлоридов
в Москве-реке на выходе из города в 4—5 раз выше, чем на входе. Вода, попавшая на
земную поверхность, частично просачивается в грунт и доходит до
водонепроницаемого слоя (как правило, глин). Так образуются подземные воды.
Пока вода фильтруется через грунт, она очищается от большинства микропримесей.
Поэтому питьевую воду для многих городов, особенно небольших, берут не из
поверхностных источников, а из подземных. Однако с глубиной минерализация воды
растёт. В частности, под Москвой на глубине 1000— 1200 м залегают крепкие
рассолы.
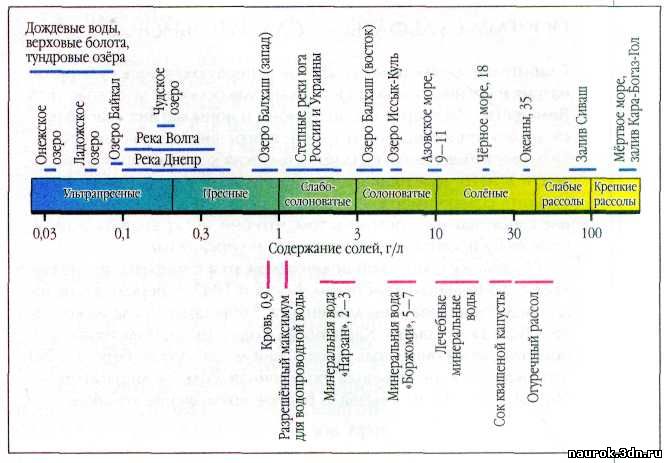
Содержание минеральных солей в водах различных водоёмов,
физиологических жидкостях и пищевых продуктах.

Реки, текущие по известнякам, насыщаются гидрокарбонатом
кальция. Берега реки Белой (Башкирия) сложены известняком.
|  З В О Н О К НА У Р О К
З В О Н О К НА У Р О К З В О Н О К НА У Р О К
З В О Н О К НА У Р О К