Цели урока: На основе универсального
понятия " гидролиз” показать единство мира
органических и неорганических веществ.
Используя интеграционный потенциал этого
понятия раскрыть внутри – и межпредметные связи
химии, дать яркое представление о практической
значении процессов гидролиза в живой и неживой
природе и в жизни общества. Ознакомить учащихся с
сущностью гидролиза солей и научить составлять
уравнения гидролиза различных солей.
Оборудование и реактивы: Растворы HCI,
HNO3, NaOH, Na2CO3, AICI3, KNO3,
FeCI3; кусочек CaC2; пробирки, штативы,
растворы индикаторов и наборы универсальной
индикаторной бумаги.
Форма урока. Лекция.
Ход урока
1. Организационный момент.
2. Объяснение нового материла (в ходе
объяснения материла, идет демонстрация опытов).
Гидролиз – реакция обменного разложения
веществ водой.
Гидролизу подвергаются: органические и
неорганические вещества.
Реакции гидролиза могут быть: обратимые и
необратимые.
- Гидролиз органических веществ:
А) гидролиз галогеналканов: C2H5CI + H2O
—> C2H5OH + HCI
Б) гидролиз сложных эфиров: CH3COOC2H5
+ H2O —> CH3COOH + C2H5OH
В) гидролиз жиров:
Г) гидролиз дисахаридов: C12H22O11
+ H2O —>C6H12O6 + C6H12O6
Д) гидролиз белков:
H2N – CH2 – CO – NH – CH2 – CO – NH – CH2
– COOH + H2O—> 3H2N – CH2COOH
Е) гидролиз полисахаридов: (C6H10O5)n
+ H2O —> n C6H12O6
Работа обучающихся по листу заданий
2. Гидролиз бинарных неорганических веществ:
А) гидролиз карбидов: CaC2 + 2H2O —> Ca(OH)2
+ C2H2
Б) гидролиз галогенидов: SiCI4 + 3 H2O —> H2SiO4
+ 4 HCI
В) гидролиз гидридов: NaH + H2O —>NaOH + H2
Г) гидролиз фосфидов: Mq3P2 + 6H2O
—>3 Mq(OH)2 + 2PH3
Д) гидролиз сульфидов: AI2S3 + 6H2O
—>2AI(OH)3 + 3 H2S.
При растворении некоторых солей в воде
самопроизвольно протекают не только диссоциация
их на ионы и гидратация ионов, но и процесс
гидролиза солей.
Гидролиз солей – это
протолитический процесс взаимодействия ионов
солей с молекулами воды, в результате которого
образуются малодиссоциирующие молекулы или
ионы.
С позиции протолитической теории
гидролиз ионов солей заключается в переходе
протона от молекулы воды к аниону соли или
катиону соли (с учетом его гидратации) к молекуле
воды. Таким образом, в зависимости от природы
иона вода выступает либо как кислота, либо как
основание, а ионы соли при этом являются
соответственно сопряженным основанием или
сопряженной кислотой.( в водном растворе соли
появляется избыток свободных H+ илиOH– и
раствор соли становится кислотным или щелочным.
Возможны три варианта гидролиза ионов
солей:
- гидролиз по аниону – соли, содержащий катион
сильного основания и анион слабой кислоты;
- гидролиз по катиону – соли, содержащие катион
слабого основания и анион сильной кислоты;
- гидролиз и по катиону, и по аниону – соли,
содержащие катион слабого основания и анион
слабой кислоты.
Рассмотрим случаи гидролиза
Гидролиз по аниону. Соли,
содержащие анионы слабых кислот, например
ацетаты, цианиды, карбонаты, сульфиды,
взаимодействуют с водой, так как эти анионы
являются сопряженными основаниями, способными
конкурировать с водой за протон, связывая его в
слабую кислоту:
A-+ H2O —> AH + OH–
pH > 7 |
|
| CH3COO– + H2O —>CH3COOH
+ OH– |
CN– + H2O —> HCN + OH- |
| CO32– + H2O —> HCO3–
+ OH– |
HCO3– + H2O —>H2 CO3
+ OH- |
| I ступень |
II ступень |
При этом взаимодействии возрастает
концентрация ионов OH-, и поэтому pH водных
растворов солей, гидролизующихся по аниону,
всегда находится в щелочной области pH > 7.
Гидролиз многозарядных анионов слабых кислот в
основном протекает по I ступени. Работа
обучающихся по листу заданий
Для характеристики состояния равновесия при
гидролизе солей используют константу гидролиза
Кг, которая при гидролизе по аниону равна:
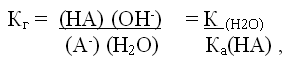
где К H2O – ионное произведение воды; Ка
– константа диссоциации слабой кислоты НА.
В соответствии с принципом Ле – Шателье
смещения химического равновесия для подавления
гидролиза, протекающего по аниону, к раствору
соли следует добавить щелочь как поставщика иона
ОН-, образующегося при гидролизе соли по
аниону (ион, одноименный продукту гидролиза).
Гидролиз по катиону. Соли, содержащие
катионы слабых оснований, например катионы
аммония, алюминия, железа, цинка, взаимодействуют
с водой, так как являются сопряженными кислотами,
способными отдавать протон молекулам воды или
связывать ионы ОН– молекул воды с
образованием слабого основания:
Kt+ + H2O —> KtOH + H+ pH
< 7
NH4+ + H2O —> NH3 + H3O+
Fe3+ + H2O —> FeOH2+ + H+ ; I
– ступень
FeOH2+ + H2O —> Fe(OH)+2 + H+
; II – ступень
Fe(OH)+2 + H2O —>Fe(OH)3 + H+ III
– ступень
При этом взаимодействии возрастает
концентрация ионов H+, и поэтому pH водных
растворов солей, гидролизующихся по катиону,
всегда находится в кислой области pH < 7.
Гидролиз многозарядных катионов слабых
оснований в основном протекает по I ступени.
Для подавления гидролиза, протекающего по
катиону, к раствору соли следует добавить
кислоту как поставщика иона Н+,
образующегося при гидролизе соли по катиону (ион,
одноименный продукту гидролиза. Работа
обучающихся по листу заданий
Гидролиз по катиону и по аниону. В этом
случае в реакции гидролитического
взаимодействия с водой участвуют одновременно и
катионы, и анионы, а реакция среды определяется
природой сильного электролита.
Если гидролиз по катиону и по аниону протекает
в равной степени (кислота и основание –
одинаково слабые электролиты), то раствор соли
имеет нейтральную реакцию; например, водный
раствор ацетата аммония NH4CH3COO имеет pH
= 7,т.к.pKa (CH3COOH) = 4,76 и pKb(NH3*H2O)
= 4,76.
Если в растворе преобладает гидролиз
по катиону (основание слабее кислоты), раствор
такой соли имеет слабокислую реакцию (pH < 7) ,
например нитрит аммония NH4NO2
(pKa (HNO2) = 3,29) .
Если в растворе преобладает гидролиз
по аниону (кислота слабее основания), раствор
такой соли имеет слабощелочную реакцию (pH > 7) ,
например цианид аммония NH4СN
(pKa (HСN) = 9,31) .
Работа обучающихся по листу заданий
Некоторые соли, гидролизующиеся по
катиону и по аниону, например сульфиды или
карбонаты алюминия, хрома, железа (III),
гидролизуются полностью и необратимо, так как
при взаимодействии их ионов с водой образуются
малорастворимые основания и летучие кислоты, что
способствует протеканию реакции до конца:
AI2(CO3)3 + 3 H2O —>2 AI(OH)3
+ 3 CO2; Cr2S3 + 6 H2O —>2 Cr(OH)3
+ 3 H2S
Механизм необратимого гидролиза
В растворах двух солей, например
сульфида натрия (Na2S) и хлорида алюминия (AICI3),
взятых порознь, устанавливается равновесие: S2–
+ H2O —> HS– + OH-
AI3+ + H2O —> AIOH2+ + H+
гидролиз ограничивается I стадией. При
смешивании этих растворов, ионы Н+ и ОН– взаимно
нейтрализуют друг друга, уход этих ионов из сферы
реакции в виде малодиссоциированной воды
смещает оба равновесия вправо и активизирует
последующие ступени гидролиза:
HS– + H2O —> H2S + ОН–
AIOH2+ + H2O —> AI(OH)+2
+ Н+
AI(OH)+2 + H2O —>
AI(OH)3 + Н+ ,
что в конечном счете приводит к
образованию слабого основания и слабой кислоты.
2AICI3 + 3 Na2S + 6 H2O —> 2
AI(OH)3 + 3 H2S + 6 NaCI
Эту особенность гидролиза подобных
солей следует обязательно учитывать при
сливании сточных вод, чтобы избежать их
вспенивания за счет образования CO2 или
отравления окружающей среды сероводородом.
Степень гидролиза (h) – количественная
характеристика гидролиза.
h = n / N * 100% ,
Степень гидролиза равна отношению
числа гидролизованных молекул соли к общему
числу растворенных молекул. зависит:
А) температуры, Б) концентрации
раствора, В) тип соли (природы основания, природы
кислоты).
Факторы, влияющие на степень
гидролиза:
Глубина протекания гидролиза солей в
значительной степени зависит и от внешних
факторов, в частности от температуры и концентрации
раствора. При кипячении растворов гидролиз
солей протекает значительно глубже, а охлаждение
растворов, наоборот, уменьшает способность соли
подвергаться гидролизу.
Увеличение концентрации большинства
солей в растворах также уменьшает гидролиз, а
разбавление растворов заметно усиливает
гидролиз солей.
Гидролиз – процесс эндотермический, в
большинстве обратимый. В соответствии с
принципом смещения химического равновесия для
подавления гидролиза– следует понизить
температуру, увеличить концентрацию исходной
соли, ввести в раствор один из продуктов
гидролиза( кислоты – Н+ , щелочи – ОН-);
для усиления гидролиза – следует повысить
температуру, разбавить раствор, связывание
какого – либо продукта гидролиза ( Н+ или ОН-)
в молекулы слабого электролита H2O
Гидролитические процессы вместе с процессами
растворения играют важную роль в обмене веществ.
С ними связано поддержание на определенном
уровне кислотности крови и других
физиологических жидкостей. Действие многих
химиотерапевтических средств связано с их
кислотно – основными свойствами и склонностью к
гидролизу. - Геохимические процессы.
- Химическая промышленность
3. Закрепление материала
Работа обучающихся по листу заданий
4. Домашнее задание
|  З В О Н О К НА У Р О К
З В О Н О К НА У Р О К З В О Н О К НА У Р О К
З В О Н О К НА У Р О К