Почти любое вещество может при известных
условиях дать кристаллы. Кристаллы можно получить из раствора или из
расплава данного вещества, а также из его паров (например, черные
ромбовидные кристаллы иода легко выпадают из его паров при нормальном
давлении без промежуточного перехода в жидкое состояние).
Начните растворять в воде столовую соль или
сахар. При комнатной температуре (20°С) вы сумеете растворить в
граненом стакане только 70 г соли. Дальнейшие добавки соли растворяться
не будут и улягутся на дне в виде осадка. Раствор, в котором дальнейшего
растворения уже не происходит,- называется насыщенным. Если изменить
температуру, то изменится и степень растворимости вещества. Всем хорошо
известно, что большинство веществ горячая вода растворяет значительно
легче, чем холодная.
Представьте себе теперь,- что вы
приготовили насыщенный раствор, скажем, сахара при температуре 30°С и
начинаете охлаждать его до 20°С. При 30°С вы смогли растворить в 100 г
воды 223 г сахара, при 20°С растворяется 205 г. Тогда при охлаждении от
30 до 20°С 18 г окажутся "лишними" и, как говорят, выпадут из раствора.
Итак, один из возможных способов получения кристаллов состоит в
охлаждении насыщенного раствора.
Можно поступить и иначе. Приготовьте
насыщенный раствор соли и оставьте его в открытом стакане. Через
некоторое время вы обнаружите появление кристалликов. Почему они
образовались? Внимательное наблюдение покажет, что одновременно с
образованием кристаллов произошло еще одно изменение - уменьшилось
количество воды. Вода испарилась, и в растворе оказалось "лишнее"
вещество. Итак, другой возможный способ образования кристаллов - это
испарение раствора.
Как же происходит образование кристаллов из раствора?
Мы сказали, что кристаллы "выпадают" из
раствора; надо ли это понимать так, что неделю кристалла не было, а в
одно какое-то мгновение Он сразу вдруг возник? Нет, дело обстоит не так:
кристаллы растут. Не удается, разумеется, обнаружить глазом самые
начальные моменты роста. Сначала немногие из беспорядочно движущихся
молекул или атомов растворенного вещества собираются в том примерно
порядке, который нужен для образования кристаллической решетки. Такую
группу атомов или молекул называют зародышем.
Опыт показывает, что зародыши чаще
образуются при наличии в растворе каких-либо посторонних мельчайших
пылинок. Всего быстрее и легче кристаллизация начинается тогда, когда в
насыщенный раствор помещается маленький кристалл-затравка. При этом
выделение из раствора твердого вещества будет заключаться не в
образовании новых кристалликов, а в росте затравки.
Рост зародыша не отличается, конечно, от
роста затравки. Смысл использования затравки состоит в том, что она
"оттягивает" на себя выделяющееся вещество и препятствует, таким
образом, одновременному образованию большого числа зародышей. Если же
зародышей образуется много, то они будут мешать друг другу при росте и
не позволят нам получить крупные кристаллы.
Как распределяются на поверхности зародыша порции атомов или молекул, выделяющихся из раствора?
Опыт показывает, что рост зародыша или
затравки заключается как бы в перемещении граней параллельно самим себе в
направлении, перпендикулярном к грани. При этом углы между гранями
остаются постоянными (мы уже знаем, что постоянство углов - важнейший
признак кристалла, вытекающий из его решетчатого строения).
На рис. 4.6 даны встречающиеся очертания
трех кристаллов одного и того же вещества при их росте. Подобные картины
можно наблюдать в микроскоп. В случае, изображенном слева, число граней
во время роста сохраняется. Средний рисунок дает пример появления новой
грани (вверху справа) и снова ее исчезновения.
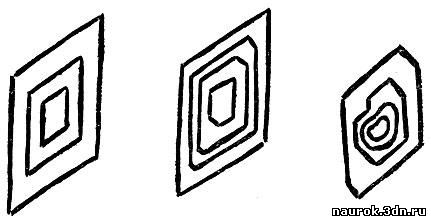
Рис. 4.6
Очень важно отметить, что скорость роста
граней, т. е. скорость перемещения их параллельно самим себе,
неодинакова у разных граней. При этом "зарастают" (исчезают) именно те
грани, которые перемещаются всего быстрее, например левая нижняя грань
на среднем рисунке. Наоборот, медленно растущие грани оказываются самыми
широкими, как говорят, наиболее развитыми.
Особенно отчетливо это видно на последнем
рисунке. Бесформенный обломок приобретает ту же форму, что и другие
кристаллы, именно из-за анизотропии скорости роста. Вполне определенные
грани развиваются за счет других всего сильнее и придают кристаллу
форму, свойственную всем образцам этого вещества.
Очень красивые переходные формы наблюдаются
в том случае, когда в качестве затравки берется шар, а раствор
попеременно слегка охлаждается и нагревается. При нагревании раствор
становится ненасыщенным, и идет частичное растворение затравки.
Охлаждение ведет к насыщению раствора и росту затравки. Но молекулы
оседают при этом по-иному, как бы отдавая предпочтение некоторым местам.
Вещество, таким образом, переносится с одних мест шара на другие.
Сначала на поверхности шара появляются
маленькие грани в форме кружков. Кружки постепенно увеличиваются и,
соприкасаясь друг с другом, сливаются по прямым ребрам. Шар превращается
в многогранник. Затем одни грани обгоняют другие, часть граней
зарастает, и кристалл приобретает свойственную ему форму (рис. 4.7).
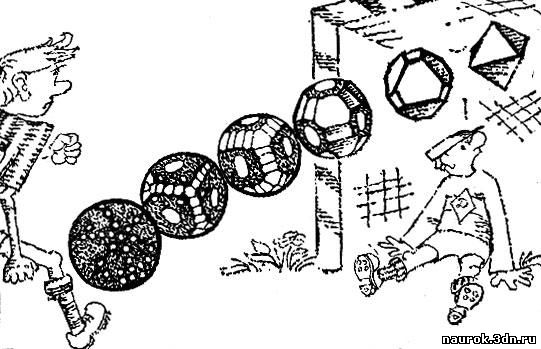
Рис. 4.7
При наблюдении за ростом кристаллов
поражает основная особенность роста - параллельное перемещение граней.
Получается так, что выделяющееся вещество застраивает грань слоями: пока
один слой не достроен, следующий строиться не начинает.
На рис. 4.8 показана "недостроенная"
упаковка атомов. В каком из обозначенных буквами положений прочнее всего
будет удерживаться новый атом, пристроившись к кристаллу? Без сомнения,
в А, так как здесь он испытывает притяжение соседей с трех сторон,
тогда как в Б - с двух, а в В - только с одной стороны. Поэтому сначала
достраивается столбик, затем вся плоскость и только потом начинается
укладка новой плоскости.
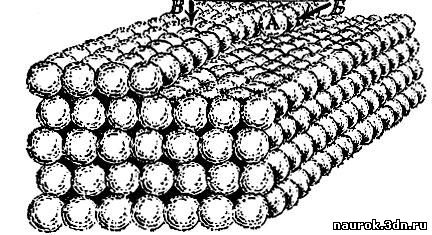
Рис. 4.8
В целом ряде случаев кристаллы образуются
из расплавленной массы - из расплава. В природе это совершается в
огромных масштабах: из огненной магмы возникли базальты, граниты и
многие другие горные породы.
Начнем нагревать какое-нибудь
кристаллическое вещество, например каменную соль. До 804°С кристаллики
каменной соли будут мало изменяться: они лишь незначительно расширяются,
и вещество остается твердым. Измеритель температуры, помещенный в сосуд
с веществом, показывает непрерывный рост температуры при нагревании.
При 804°С мы обнаружим сразу два новых, связанных между собой явления:
вещество начнет плавиться, и подъем температуры приостановится. Пока все
вещество не превратится в жидкость,; температура не изменится;
дальнейший подъем температуры - это уже нагревание жидкости. Все
кристаллические вещества имеют определенную температуру плавления. Лед
плавится при 0°С, железо - - при 1527°С, ртуть - при -39°С и т. д.
Как мы уже знаем, в каждом кристаллике
атомы или молекулы вещества образуют упорядоченную Г упаковку и
совершают малые колебания около своих средних положений. По мере
нагревания тела скорость колеблющихся частиц возрастает вместе с
размахом колебаний. Это увеличение скорости движения частиц с
возрастанием температуры составляет один из основных законов природы,
который относится к веществу в любом состоянии - твердом, жидком или
газообразном.
Когда достигнута определенная, достаточно
высокая температура кристалла, колебания его частиц становятся столь
энергичными, что аккуратное расположение частиц становится невозможным -
кристалл плавится. С началом плавления подводимое тепло идет уже не на
увеличение скорости частиц, а на разрушение кристаллической решетки.
Поэтому подъем температуры приостанавливается. Последующее нагревание -
это увеличение скорости частиц жидкости.
В интересующем нас случае кристаллизации из
расплава вышеописанные явления наблюдаются в обратном порядке: по мере
охлаждения жидкости ее частицы замедляют свое хаотическое движение; при
достижении определенной, достаточно низкой температуры скорость частиц
уже столь мала, что некоторые из них под действием сил притяжения
начинают пристраиваться одна к другой, образуя кристаллические зародыши.
Пока все вещество не закристаллизуется, температура остается
постоянной. Эта температура, как правило, та же, что и температура
плавления.
Если не принимать специальных мер, то
кристаллизация из расплава начнется сразу во многих местах. Кристаллики
будут расти в виде правильных, свойственных им многогранников совершенно
так же, как мы это описывали выше. Однако свободный рост продолжается
недолго: увеличиваясь, кристаллики наталкиваются друг на друга, в местах
соприкосновения рост прекращается, и затвердевшее тело получает
зернистое строение. Каждое зерно - это отдельный кристаллик, которому не
удалось принять своей правильной формы.
В зависимости от многих условий, и прежде
всего от быстроты охлаждения, твердое тело может обладать более или
менее крупными зернами: чем медленнее охлаждение, тем крупнее зерна.
Размеры зерен кристаллических тел колеблются от миллионной доли
сантиметра до нескольких миллиметров. В большинстве случаев зернистое
кристаллическое строение можно наблюдать в микроскоп. Твердые тела
обычно имеют именно такое мелкокристаллическое строение.
Для техники представляет очень большой
интерес процесс застывания металлов. События, происходящие при литье и
при застывании металла в формах, физики исследовали чрезвычайно
детально.
Большей частью при затвердевании растут
древоподобные монокристаллики, носящие название дендритов. В иных
случаях дендриты ориентированы как попало, в других случаях -
параллельно друг другу.
На рис. 4.9 показаны стадии роста одного
дендрита. При таком поведении дендрит может зарасти прежде, чем он
встретится с другим аналогичным. Тогда в отливке мы не найдем дендритов.
События могут развиваться и иначе: дендриты могут встретиться и
прорастать друг в друга (ветки одного в промежутки между ветками
другого), пока они еще "молоды".

Рис. 4.9
Таким образом, могут возникнуть отливки,
зерна которых (показанные на рис. 2.22) обладают самой различной
структурой. А от характера этой структуры существенно зависят свойства
металлов. Управлять поведением металла при затвердевании можно, меняя
скорость охлаждения и систему отвода тепла.
θТеперь поговорим о том, как вырастить
крупный одиночный кристалл. Ясно, что требуется принять меры к тому,
чтобы кристалл рос из одного места. А если уж начало расти несколько
кристалликов, то во всяком случае надо сделать так, чтобы условия роста
были благоприятны лишь для одного из них.
Вот, например, как поступают при
выращивании кристаллов легкоплавких металлов. Металл расплавляют в
стеклянной пробирке с оттянутым концом. Пробирку, подвешенную на нити
внутри вертикальной цилиндрической печи, медленно опускают вниз.
Оттянутый конец постепенно выходит из печи и охлаждается. Начинается
кристаллизация. Сначала образуется несколько кристалликов, но те,
которые растут вбок, упираются в стенку пробирки и рост их замедляется. В
благоприятных условиях окажется лишь тот кристаллик, который растет
вдоль оси пробирки, т. е. в глубь расплава. По мере опускания пробирки
новые порции расплава, попадающие в область низких температур, будут
"питать" этот единственный кристалл. Поэтому из всех кристалликов
выживает он один; по мере опускания пробирки он продолжает расти вдоль
ее оси. В конце концов весь расплавленный металл застывает в виде
одиночного кристалла.
Та же идея лежит в основе выращивания
тугоплавких кристаллов рубина. Мелкий порошок вещества сыплют струей
через пламя. Порошинки при этом плавятся; крошечные капли падают на
тугоплавкую подставку очень малой площади, образуя множество
кристалликов. При дальнейшем падении капель на подставку все кристаллики
растут, но опять-таки вырастает лишь тот из них, который находится в
наиболее выгодном положении для "приема" падающих капель.
Для чего же нужны крупные кристаллы?
В крупных одиночных кристаллах часто
нуждаются промышленность и наука. Большое значение для техники имеют
кристаллы сегнетовой соли и кварца, обладающие замечательным свойством
преобразовывать механические действия (например, давление) в
электрическое напряжение.
Оптическая промышленность нуждается в крупных кристаллах кальцита, каменной соли, флюорита и др.
Для часовой промышленности нужны кристаллы
рубинов, сапфиров и некоторых других драгоценных камней. Дело в том, что
отдельные подвижные части обыкновенных часов делают в час до 20 000
колебаний. Такая большая нагрузка предъявляет необычайно высокие
требования к качеству кончиков осей и подшипников. Истирание будет
наименьшим, когда подшипником для кончика оси диаметром 0,07-0,15 мм
служит рубин или сапфир. Искусственные кристаллы этих веществ очень
прочны и очень мало истираются сталью. Замечательно, что искусственные
камни оказываются при этом лучше таких же природных камней.
Однако наибольшее значение для промышленности имеет выращивание монокристаллов полупроводников - кремния и германия.
|  З В О Н О К НА У Р О К
З В О Н О К НА У Р О К З В О Н О К НА У Р О К
З В О Н О К НА У Р О К